рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Философия
- /
- Генетический контроль молекул антигенраспознающих рецепторов Т-лимфоцитов
Реферат Курсовая Конспект
Генетический контроль молекул антигенраспознающих рецепторов Т-лимфоцитов
Генетический контроль молекул антигенраспознающих рецепторов Т-лимфоцитов - раздел Философия, Определение иммунологии, основные ее понятия Организация Генов, Кодирующих A И B Цепи Т-Клеточных Рецептор...
Организация генов, кодирующих a и b цепи Т-клеточных рецепторов во многом аналогична таковой для легких и тяжелых цепей иммуноглобулинов в В-лимфоцитах. Так, a-цепь Т-клеточных рецепторов кодируется набором сцепленных генов, аналогичным таковому для легких цепей иммуноглобулинов в В-лимфоцитах. В частности, вариабельный домен a-цепи кодируют:
Ø 100 V-генов, каждый из которых кодирует бóльшую часть вариабельного домена a-цепи определенной специфичности. Каждому V-гену предшествует короткий L-генный фрагмент, кодирующий короткий гидрофобный лидерный фрагмент, необходимый для прохождения Т-клеточного рецептора через мембрану гранулярного эндоплазматического ретикулума и плазматическую мембрану. В зрелой молекуле Т-клеточного рецептора, находящейся на поверхности Т-лимфоцита этот лидерный гидрофобный пептидный участок отсутствует
Ø 50 J-генов, кодирующих меньшую часть вариабельного домена.
Константный домен a-цепиТ-клеточного рецептора кодируется одним С-геном, включающим 3 экзона (информационных участка), которые соответственно кодируют:
Ø собственно константный домен
Ø шарнирную область
Ø трансмембранный (гидрофобный) и цитоплазматический (хвостовой) участки a-цепи.
b-цепь Т-клеточных рецепторов кодируется набором генов, аналогичным таковому для тяжелых цепей иммуноглобулинов. В частности, вариабельныйиконстантный домены этой цепи кодируют следующие гены:
Ø 30 V-генов, каждый из которых кодирует бóльшую часть вариабельного домена b-цепи определенной специфичности
Ø 2 генных кластера, включающих гены DJC. Причем каждый генный кластер включает один Dи 6 J-генных сегментов.Функциональные различия между этими двумя генными кластерами не известны, также как и не известно функциональное значение такого дублирования генных кластеров. С-ген для b-цепи состоит из 4 экзонов, которые соответственно кодируют:
ü собственно константный домен
ü шарнирный участок
ü трансмембранный (гидрофобный) участок
ü хвостовой (цитоплазматический) участок.
Процессы рекомбинации, транскрипции, сплайсинга и трансляции генетического материала для a- и b-цепей при образовании антигенраспознающих рецепторов Т-лимфоцитов аналогичны тем, что происходят в В-лимфоцитах при синтезе иммуноглобулинов. В частности, структура вариабельного домена a-цепи Т-клеточного рецептора во многом зависит от случайной рекомбинации какого-то одного из 100 V-генов с каким-то одним из 50 J-геном, которая осуществляется путем делеции участка ДНК между этими генами. В результате такой делеции возникает определенный ViJi-локус, кодирующий вариабельный домен a-цепи. Затем пре-мРНК, комплементарная ViJi-локусу ДНК, в процессе сплайсинга объединяется с пре-мРНК, комплементарной С-гену для a-цепи, в результате чего формируется зрелая мРНК, кодирующая a-цепь, которая и транслируется.
При синтезе b-цепи Т-клеточных рецепторов в геноме Т-лимфоцитов происходит случайная рекомбинация какого-то одного из 30 V-генов с одним из двух генных кластеров DJ-генов. При этом внутри самого DJ-генного кластера осуществляется рекомбинация между D-геном и каким-то одним из 6 J-генов. В результате отмеченных соматических рекомбинаций возникает определенный ViDJi-локус, кодирующий синтез вариабельного домена b-цепи определенной специфичности. Затем в процессе сплайсинга пре-мРНК, комплементарная ViDJi-локус ДНК, объединяется с пре-мРНК, комплементарной С-гену для b-цепи, в результате чего формируется зрелая мРНК, кодирующая b-цепь с определенной специфичностью вариабельного домена.
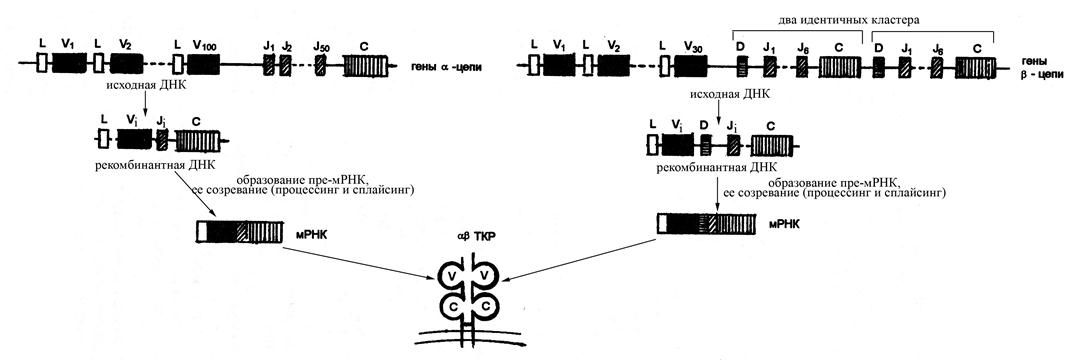
Рис. Организация генов, кодирующих α- и β-цепи антигенраспознающего рецептора Т-лимфоцитов. Принцип реорганизации генных сегментов, контролирующих α- и β-цепи Т-клеточного рецептора, аналогичен таковому для иммуноглобулинов. Отличие состоит в том, что локус для β-цепи имеет два идентичных кластера. В чем функциональное значение такого дублирования, неизвестно
Несмотря на описанное сходство в генетическом контроле Т-клеточных рецепторов Т-лимфоцитов и иммуноглобулинов В-лимфоцитов, которое заключается в многообразии генов, кодирующих вариабельные домены, а также процессах соматической рекомбинации генома и последующего созревания мРНК, все же в генетическом контроле Т-клеточных рецепторов имеются некоторые особенности. Эти особенности обусловлены тем, что Т-клеточный рецептор, в отличие от иммуноглобулиновых рецепторов В-лимфоцитов, распознает не нативный антигенный эпитоп, а его комплекс с относительно мало изменчивыми молекулами МНС. В частности, в вариабельном домене a- и b-цепей Т-клеточного рецептора имеются по 3 петлеобразные гипревариабельные области, называемые CDR-участками (от англ. complementary determining region). Первые две из этих гипервариабельных петель занимают периферию домена и ответственны за взаимодействие с a-спиральными участками двух антигенсвязывающих доменов МНС, ограничивающих собой антигенсвязывающую щель молекулы МНС. Третьи гипервариабельные петли a- и b-цепей Т-клеточного рецептора при формировании его антигенсвязывающего центра оказываются расположенными во внутренней части этого центра и собственно и обеспечивают взаимодействие с антигенным эпитопом, фиксированном между a-спиральными участками антигенсвязывающего центра молекулы МНС. CDR1- и CDR2 -участки вариабельных доменов a- и b-цепей Т-клеточного рецептора кодируются преимущественно V-геном, тогда как большая часть CDR3-участка – J-геном. В связи со сравнительно небольшой изменчивостью антигенсвязывающих участков молекул МНС, нет необходимости в большой изменчивости CDR1- и CDR2 -участков вариабельных доменов a- и b-цепей Т-клеточного рецептора, которые ответственны за связь с антигенсвязывающими участками молекул МНС. Это, вероятно, и является причиной гораздо меньшего в сравнении с В-лимфоцитами, разнообразия V-генов, кодирующих вариабельные домены a- и b-цепей Т-клеточного рецептора в Т-лимфоцитах. Вместе с тем J-гены, кодирующие CDR3-области вариабельных доменов a- и b-цепей Т-клеточного рецептора, отличаются гораздо большим разнообразием, по сравнению с таковыми генами, кодирующими иммуноглобулины, поскольку CDR3-области Т-клеточных рецепторов как раз и ответственны за взаимодействие с антигенным эпитопом.
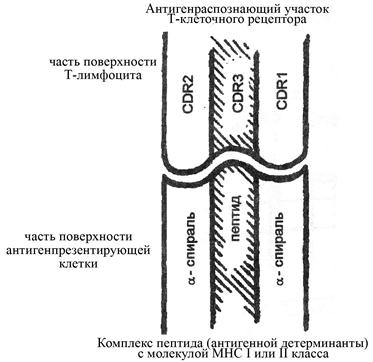
Рис. Принцип структурных отношений между гипервариабельными участками (СDR-участками) антигенраспознающего рецептора Т-лимфоцита и комплексом "антигенная детерминанта - молекула МНС" антигенпрезентирующей клетки. Гипервариабельные участки Т-клеточного рецептора конформационно организованы так, что наиболее вариабельный регион (СDR3) локализован в центре антигенраспознающего участка. При этом распознаваемый антигенный пептид также находится в центре комплекса между α-спиральными последовательностями молекулы МНС. СDR1 и СDR2 участки антигенраспознающего домена Т-клеточного рецептора, характеризующиеся сравнительно меньшей вариабельностью (по сравнению СDR3), ответственны за взаимодействие с α-спиральными участками антигенсвязывающего домена молекулы МНС. Подобная конформационная особенность Т-клеточного рецептора обеспечивает наиболее эффективное распознавание антигенного пептида в комплексе с молекулой МНС
Т-клеточный рецептор, фиксированный в мембране Т-лимфоцитов, подобно иммуноглобулиновым рецепторам В-лимфоцитов, имеет очень короткий цитоплазматический хвост, в связи с чем не способен сам по себе активировать внутриклеточные ферменты и вызывать активацию Т-лимфоцитов. Для активации Т-лимфоцита и последующего его превращения в зрелую форму необходимы специальные трансмиссивные белки, часть из которых ассоциирована с Т-клеточным рецептором, а часть – расположена на некотором удалении от него. В частности, с Т-клеточным рецептором ассоциировано 5 белков, получивших общее название СD3:
Ø СD3g, СD3d, СD3e, расположенных на поверхности Т-лимфоцита, фиксированных в его мембране. Эти белки имеют гомологию с иммуноглобулинами: у каждого такого белка имеется внеклеточный глобулярный домен и сравнительно длинный участок, включающий трансмембранную и цитоплазматическую части (причем цитоплазматический хвост этих белков является гораздо более длинным по сравнению с таковым самого Т-клеточного рецептора, что позволяет этим белкам вступать во взаимодействие с цитоплазматическими белками, активируя их). Эти белки находятся на клеточной поверхности в ассоциированном друг с другом состоянии – в виде гетеродимеров СD3ed и СDeg. Связь таких гетеродимеров с Т-клеточным рецептором осуществляется посредством электростатического притяжения: отрицательно заряженные трансмембранные участки этих белков притягиваются положительно заряженным трансмембранным участком Т-клеточного рецептора.
Ø СD3z и СD3h. Каждый из этих белков имеет глобулярный домен, расположенный в цитоплазме Т-лимфоцита и обладающий способностью взаимодействовать с определенными цитоплазматическими белками-трансдукторами, активируя их, и трансмембранный хвостовой участок, обеспечивающий фиксацию этих белков в мембране в непосредственной близости от Т-клеточного рецептора. СD3z и СD3h-белки, подобно СD3g, СD3d, СD3e, находятся в ассоциированном друг с другом состоянии – в виде димеров СD3zz (гомодимер) и СD3zh (гетеродимер). Функциональные различия между этими димерами не известны. Около 80% Т-клеточного рецептора ассоциировано с гомодимером СD3zz и 20% – с гетеродимером СD3zh.
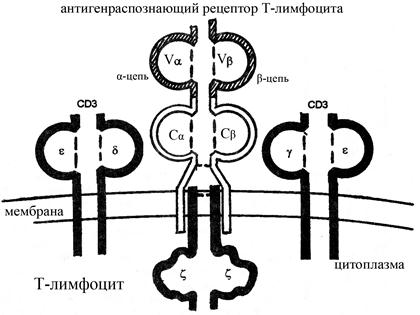
Рис. Схема строения антигенраспознающего Т-клеточного рецептора. Комплекс включает Т-клеточный антигенраспознающий рецептор и 5 однодоменных инвариантных СD3-белков: γ, d, e находятся на поверхности Т-лимфоцита, тогда как z и h погружены в цитоплазму; h на рисунке не показан. Белки γ, d, e, имеющие удлиненный цитоплазматический хвост, служат для передачи сигнала внутрь клетки после взаимодействия антигенраспознающего рецептора Т-лимфоцита с антигеном
Помимо сигналпередающей функции все пять СD3 белков играют важную роль в процессе транспорта Т-клеточного рецептора на поверхность Т-лимфоцитов. Так, у мутантных клеток с полностью отсутствующим синтезом g-, d- и e-белков выход Т-клеточного рецептора на поверхность Т-лимфоцита полностью нарушен, хотя внутриклеточный синтез молекул Т-клеточного рецептора осуществляется. При мутациях гена, кодирующего z-белок, выход Т-клеточного рецептора на поверхность клетки происходит в меньшей степени по сравнению с нормой.
Наряду с пятью СD3-белками, ассоциированными с Т-клеточным рецептором, в активации Т-лимфоцита после его контакта с антигеном принимает участие и другой белок, фиксированный в плазматической мембране, однако находящийся на некотором удалении от комплекса Т-клеточного рецептора с СD3-белками.
Для Т-лимфоцитов-киллеров (цитотоксических Т-лимфоцитов) таким белком служит белок, получивший название СD8 (он же считается специфическим маркером Т-киллеров, в связи с чем их называют еще СD8-клетки).
В Т-хелперах и Т-клетках воспаления подобный белок, принимающий участие в активации этих клеток, но несколько отличающийся по строению, носит название СD4-белка (также считается специфическим маркером этих клеток, в связи с чем Т-хелперы и Т-клетки воспаления называют СD4-клетки).
Молекула СD4-белкаТ-хелперов и Т-клеток воспаления является одноцепочечной и включает
ü 4 глобулярных домена: D1, D2, D3 и D4
ü и хвостовой участок, часть которого является трансмембранной (обеспечивает фиксацию молекулы в плазматической мембране), а часть – цитоплазматической (достаточно длинная, имеет возможность взаимодействовать с определенными клеточными белками-трансдукторами, активируя их).
Между доменами D2 и D3 молекулы СD4имеется шарнирный участок, проявляющий большую конформационную гибкость. Домен D1 обладает способностью взаимодействовать с b2-доменом молекулы МНС II класса; предполагается также слабое включение во взаимодействие с молекулой МНС и D2-домена молекулы СD4. Таким образом, СD4-белок Т-хелперови Т-клеток воспалениявыполняет функцию корецептора для антигенраспознающего рецептора этих Т-лимфоцитов: а именно, после распознавания Т-клеточным рецептором антигенной детерминанты, связанной с молекулой МНС II класса антигенпредставляющей клетки (макрофага), происходит не только взаимодействие антигенсвязывающей области Т-клеточного рецептора с антигенной детерминантой, но и присоединение доменов D1 и D2 белка СD4к b2-домену молекулы МНС II класса. При этом белок СD4 Т-хелперови Т-клеток воспалениянесколько изменяет свою конформацию в результате такого взаимодействия с молекулой МНС, активируется и начинает активировать определенные цитоплазматические белки-трансдукторы.
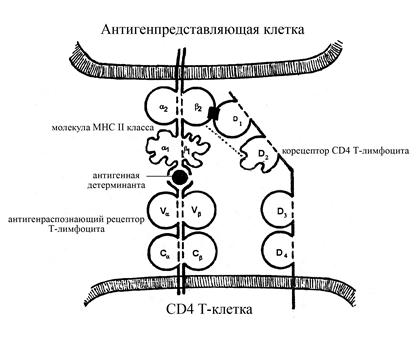
Рис. Распознавание СD4 Т-клетками (Т-хелперами или Т-клетками воспаления) комплекса "антигенный пептид - молекула МНС II класса". После распознавания Т-клеточным рецептором комплекса "антигенный пептид - молекула МНС II класса" в реакцию взаимодействия вступает корецептор СD4 (служащий специфическим маркером Т-хелперов и Т-клеток воспаления). Взаимодействие происходит между β2-доменом молекулы МНС II класса и D1-доменом корецептора СD4. Корецептор имеет достаточно длинный цитоплазматический хвост, который передает сигнал о взаимодействии Т-клеточного рецептора с антигенным комплексом внутрь Т-лимфоцита
Аналогичную функцию корецептора антигенраспознающего рецептора в Т-киллерах выполняет белок СD8,который представляет собой гетеродимер и состоит из двух цепей – a и b. Каждая из этих цепей включает
ü один глобулярный иммуноглобулиноподобный домен
ü и длинный хвостовой участок, часть которого находится над поверхностью мембраны Т-лимфоцита и проявляет высокую конформационную гибкость (шарнирный надмембранный участок), часть – является трансмембранной, а часть – представляет собой достаточно длинный цитоплазматический хвост, который обладает способность взаимодействовать с определенными внутриклеточными белками-трансдукторами, активируя их.
Глобулярные домены a- и b-цепей белка СD8 Т-киллеровобладают способностью вступать во взаимодействие с a3-доменом тяжелой a-цепи молекулы МНС I класса антигенпредставляющих клеток.
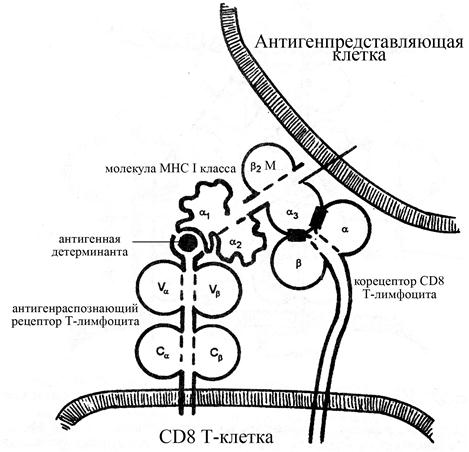
Рис. Распознавание CD8 Т-клетками (Т-киллерами) комплекса "антигенный пептид - молекула МНС I класса". В процесс распознавания вступает Т-клеточный рецептор и корецептор СD8 (специфический маркер Т-киллеров). Причем СD8 взаимодействует своими α- и β-доменами с a3-доменом молекулы МНС I класса. СD8, как и СD4, имеет относительно длинный цитоплазматический хвост, который позволяет ему передавать сигнал о взаимодействии внутрь клетки
Таким образом, наличие молекул СD8на поверхности Т-киллеров делает возможным их взаимодействие только с теми антигенными детерминантами, которые связаны с молекулами I класса МНС, тогда как маркеры СD4 Т-хелперови Т-клеток воспаленияобуславливают возможность взаимодействия этих клеток только с антигенными детерминантами, ассоциированными с молекулами II класса МНС антигенпредставляющих клеток.
Внутриклеточные события, определяющие активацию Т-лимфоцитов после взаимодействия их рецепторов с антигенными детерминантами, аналогичны тем, которые происходят в В-лимфоцитах после антигенной стимуляции. В частности, образовавшийся агрегат из антигенпредставляющих молекул МНС I или II класса, самой антигенной детерминанты, Т-клеточного рецепторного комплекса, включающего Т-клеточный рецептор, молекулы СD3 и СD4 или СD8, провоцирует внутриклеточное взаимодействие различных тирозинкиназ с цитоплазматической частью пептидов Т-клеточного рецепторного комплекса. Причем среди СD3-белков наибольшей связывающей способностью в отношении тирозинкиназ обладают белки СD3z и СD3h, главные домены которых обращены в цитоплазму Т-лимфоцита. Активированные в результате взаимодействия с белками Т-клеточного рецепторного комплекса тирозинкиназы обеспечивают каскад реакций, следствием которых является индукция специфической транскрипции определенных генов Т-лимфоцита:
Ø генов, кодирующих синтез Т-зависимых лимфокинов (например, интрелейкина-2 Т-хелперами, который в свою очередь, способствует превращению В-лимфоцитов в плазматические клетки)
Ø генов, ответственных за регуляцию пролиферации и дифференцировки Т-хелперов и Т-киллеров до стадии зрелых функционально активных клеток.
– Конец работы –
Эта тема принадлежит разделу:
Определение иммунологии, основные ее понятия
МОРФО ФУНКЦИОНАЛЬНАЯ ХАРАКТЕРИСТИКА ИММУННОЙ СИСТЕМЫ Общая морфо функциональная характеристика иммунной... МЕХАНИЗМЫ НЕСПЕЦИФИЧЕСКОГО ИММУНИТЕТА... Понятие о неспецифическом иммунитете...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Генетический контроль молекул антигенраспознающих рецепторов Т-лимфоцитов
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов