ГАЗОВЫЕ СМЕСИ - Конспект Лекций, раздел Науковедение, КОНСПЕКТЫ ЛЕКЦИИ ПО ДИСЦИПЛИНЕ ЛЕКЦИЯ 1 ОСНОВНЫЕ ПОЛОЖЕНИЯ
В Практике В Качестве Рабочего Тела Используют, Как Правило, ...
В практике в качестве рабочего тела используют, как правило, не какой-либо однородный газ, а газовую смесь: воздух, продукты сгорания различных видов топлива, природные газы и т. п. Газовая смесь – это механическая смесь газов, в которой не происходит никаких химических реакций.
Газовые смеси рассматриваются как смеси идеальных газов, подчиняющиеся законам идеальных газов, закону Дальтона, а также уравнению состояния Менделеева-Клапейрона.
Закон Дальтона гласит: общее давление смеси равно сумме парциальных давлений отдельных газов, входящих в смесь
р = р1 + р2 + р3 +р4 +… + рn, (18)
где р1, р2 …, рn – парциальные давления.
Парциальное давление – это давление, которое имел бы каждый газ, входящий в состав смеси, если бы он находился один в том же количестве, в том же объеме и при той же температуре, что и в смеси.
Если при определенной температуре смеси поднять давление какого-либо из ее компонентов (входящего в состав смеси) до давления смеси, то он займет объем, называемый парциальным.
При расчете газовой смеси надо знать значения величин, характеризующих ее газовую постоянную – Rсм, плотность rсм, молекулярную массу (кажущуюся) mсм и др.
Состав смеси может быть задан или массами компонентов, или их объемами, или массовыми и объемными долями. Иногда состав газовой смеси задается числом молей отдельных газов.
Массовой долей называется отношение массы отдельного газа, входящего в состав смеси, к массе всей смеси. Если обозначить буквами g1, g2, g3,… gn массовые доли отдельных газов смеси, а буквами G1, G2, G3 …, Gn – массы этих газов, то массовые доли каждого из n газов смеси составят
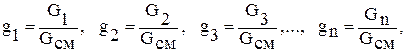
где Gсм = G1 + G2 + G3 +…+ Gn .
Очевидно, что сумма массовых долей равна единице
g1 + g2 + g3 +…+ gn = 1.
Объемной долей называется отношение парциального объема отдельного компонента смеси к полному объему смеси.
Если обозначить буквами r1, r2, r3,… rn объемные доли отдельных газов, а буквами V1, V2, V3, …, Vn – приведенные (парциальные) объемы этих газов, то объемные доли 1, 2, 3, …, i-го газа смеси составят
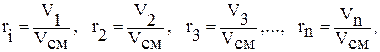 (19)
(19)
где Vсм – объем смеси:
Vсм = V1 + V2 +V3 +… + Vn .
Значит, полный объем смеси Vсм равен сумме парциальных объемов ее компонентов. Из приведенных выше уравнений следует, что r1 + r2 + r3 +…+ rn = 1.
Способ задания смеси числом молей тождествен заданию объемными долями.
Между массовыми и объемными долями существуют простые соотношения. Они позволяют производить пересчет состава смеси, заданной массовыми долями, в объемные, и наоборот:
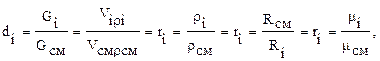 (20)
(20)
где ri, mi, Ri, rсм, mсм, Rсм – соответственно плотность, молекулярная масса, газовая постоянная i-го компонента, плотность смеси, кажущаяся молекулярная масса и газовая постоянная смеси. Молекулярная масса смеси названа здесь кажущейся в связи с условностью этого понятия для смеси газов со своими молекулярными массами.
Согласно закону Авогадро, плотности газов пропорциональны их молекулярными массам. Поэтому, решив уравнение (20), имеем:
mсм = ri mi + r2m2 +…+ rn mn.
Газовая постоянная смеси Rсм может быть определена по уравнению:
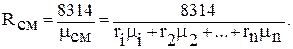 (21)
(21)
П р и м е р 1. Определить плотность кислорода и азота при нормальных условиях (760 мм рт. ст., 0 0С).
Р е ш е н и е. По формуле (13) имеем:
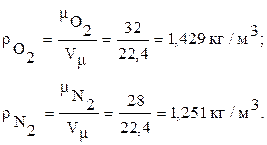
П р и м е р 2. Определить плотность кислорода при r = 8 МПа и t = 127 0C.
Р е ш е н и е. По уравнению (14):
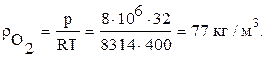
П р и м е р 3. Атмосферный воздух содержит 20,97% кислорода, 0,03 – углекислого газа и 79% – азота. При нормальных условиях определить плотность и кажущуюся молекулярную массу смеси.
Р е ш е н и е.
rсм = (rr)O2+ (rr)CO2+ (rr)N2= 0,2097 . 1,429 + 0,0003 . 1,964 +
+ 0,79 . 1,251 » 1,293 кг/м3;
rсм = (rm)O2+ (rm)CO2+ (rm)N2= 0,2097 . 32 + 0,0003 . 44 +
+ 0,79 . 28 » 28,95 кг/м3.
Контрольные вопросы и задания. 1. Напишите уравнение состояния идеального газа для 1 кг и для произвольной массы. 2. Чем отличается реальный газ от идеального? 3. Как определить газовую постоянную отдельного газа, имея универсальную газовую постоянную? 4. Дайте понятие закона Дальтона. 5. Объясните, что такое парциальное давление и парциальный объем газа. 6. Как определить плотность газовой смеси при задании ее объемными долями?
Все темы данного раздела:
ТЕРМОДИНАМИКИ И ЕЕ ЗАДАЧИ
Процессы обмена энергией имеют место в любых явлениях окружающего мира. Поэтому термодинамика как наука о взаимном превращении теплоты и работы дает методы изучения энергетических я
СОСТОЯНИЯ РАБОЧЕГО ТЕЛА
Термодинамическая система представляет собой совокупность материальных тел, находящихся в механическом и тепловом взаимодействии друг с другом и с окружающими телами. Термоди
И РЕАЛЬНЫХ ГАЗОВ
Реальные газы при низких давлениях близки к идеальным, так как в этом случае можно пренебречь силами межмолекулярного взаимодействия и объемом молекул. Это относится, в частности, к кислороду, возд
ИСТИННАЯ И СРЕДНЯЯ ТЕПЛОЕМКОСТИ
Теплоемкости могут быть массовые, объемные, молярные. Теплоемкость 1 кг газа называется массовой: она обозначается буквой с и измеряется в Дж/(кг . К).
Те
ТЕПЛОЕМКОСТИ ИДЕАЛЬНОГО ГАЗА
Как указывалось выше, температура газа при одном и том же количестве сообщаемой теплоты q изменяется по-разному в зависимости от характера термодинамического процесса. Это означает,
Значения молярных теплоемкостей и коэффициента k в зависимости от атомности
Газ
mсJ
mср
mсJ
mср
k
ТЕПЛОЕМКОСТЬ ГАЗОВЫХ СМЕСЕЙ
Теплоемкость газовой смеси, как и отдельных газов, может быть отнесена к 1 кг, 1 м3 или 1 кмолю.
Если смесь задана массовыми долями, то ее массовую теплоемкость
ТЕРМОДИНАМИЧЕСКИЙ ПРОЦЕСС
В результате воздействия на рабочее тело (газ, пар) внешней среды, например сжатия, расширения, нагрева и т. д. происходит изменение параметров его состояния.
Всякое измене
И ВНУТРЕННЯЯ ЭНЕРГИЯ
Работа совершается только при изменении объема газа. Если происходит расширение газа, то работа совершается против внешних сил; при сжатии, наоборот, газ воспринимает работу
ТЕПЛОТА
Теплота является формой движения мельчайших частиц тела. Передача теплоты от одного тела к другому осуществляется либо путем непосредственного контакта между ними (теплопроводность,
ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
Первый закон термодинамики представляет собой частный случай всеобщего закона сохранения и превращения энергии применительно к тепловым процессам.
Формулировка первого зако
ТЕРМОДИНАМИЧЕСКИЕ ПРОЦЕССЫ В ГАЗАХ
Всякое изменение состояния рабочего тела (газа) в общем случае характеризуется изменением его основных параметров: r, J, T. Состояние газа изменяется двумя путями: сообщением ему те
ЭНТРОПИЯ ГАЗОВ
При исследовании все процессы рассматриваются как равновесные и обратимые.
Прежде чем рассматривать порядок исследования термодинамических процессов, введем пятый параметр
ИЗОХОРНЫЙ ПРОЦЕСС
Процесс, протекающий при постоянном удельном объеме, называется изохорным. Изохорный процесс применяется, в частности, при расчетах теоретических циклов карбюраторных двигате
ИЗОБАРНЫЙ ПРОЦЕСС
Процесс, протекающий при постоянном давлении, называется изобарным. Такой термодинамический процесс может протекать в цилиндре, поршень которого перемещается без трения, так
ЭНТАЛЬПИЯ ГАЗА
В процессах, связанных с расчетом котельных установок, паровых турбин, а также с сушкой и охлаждением сельскохозяйственной продукции, используют параметр состояния рабочего тела (га
ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС
Процесс, протекающий при постоянной температуре рабочего тела, называется изотермическим. Он возможен, например, в цилиндре поршневой машины, если по мере подвода теплоты q к рабоче
АДИАБАТНЫЙ ПРОЦЕСС
Адиабатным называется процесс, который осуществляется без теплообмена между газом и внешней средой (q = 0). Практическое использование этот процесс находит в соплах паровых т
ПОЛИТРОПНЫЙ ПРОЦЕСС
Во всех реальных тепловых машинах (двигателях внутреннего сгорания – ДВС, компрессорах, газотурбинных установках и т. д.) процессы сжатия рабочего тела (газа), горения топлива, расш
Результаты анализа политропных процессов
Группа
Пределы
изменения
показателя
политропы
Изменение внутренней энергии
Подвод (отвод) теплоты
Теплое
КРУГОВЫЕ ПРОЦЕССЫ
Замкнутый процесс, в результате которого газ, пройдя ряд различных состояний, возвращается в исходное, называется круговым процессом (циклом).
Поясним данное определ
ПРЯМОЙ ОБРАТИМЫЙ ЦИКЛ КАРНО
В 1824 г. С. Карно предложил цикл, которому было присвоено его имя. Прямой обратимый (то есть состоящий только из равновесных, обратимых процессов) цикл Карно является идеальным цик
ОБРАТНЫЙ ОБРАТИМЫЙ ЦИКЛ КАРНО
Этот цикл является идеальным циклом холодильных машин. Изображение обратного цикла Карно приведено на рисунке 10. Цикл состоит из тех же процессов, что и прямой цикл, но состояние р
ВТОРОГО ЗАКОНА ТЕРМОДИНАМИКИ
Первый закон термодинамики устанавливает эквивалентность теплоты и работы как двух форм передачи энергии. Однако этот закон ничего не говорит об условиях преобразования теплоты и ра
КОМПРЕССОРОВ
Двигателями внутреннего сгорания (ДВС) называются тепловые поршневые машины, в которых в качестве рабочего тела используются продукты сгорания жидких или газообразных топлив, сжигае
ДВИГАТЕЛЕЙ ВНУТРЕННЕГО СГОРАНИЯ
Для анализа работы ДВС и определения основных показателей (индикаторная мощность, механический КПД) на работающем цилиндре записывают с помощью индикатора индикаторную диаграмму, пр
ЦИКЛЫ ГАЗОТУРБИННЫХ УСТАНОВОК
Газотурбинные установки (ГТУ) по сравнению с ДВС имеют существенное преимущество – отсутствие в ГТУ механизмов с возвратно-поступательным движением позволяет строить их быстроходным
ПОРШНЕВЫХ КОМПРЕССОРОВ
Сжатый воздух находит широкое применение в технологических процессах, в частности для привода пневмомеханизмов, молотов, вибраторов, пневмоподъемников, для транспортировки сыпучих м
ВОДЯНОЙ ПАР
Водяной пар в качестве рабочего тела находит широкое применение в паровых турбинах, являющихся основными тепловыми двигателями на тепловых и атомных электростанциях.
В каче
RV- И Ts-ДИАГРАММЫ ВОДЯНОГО ПАРА
Парообразование может осуществляться путем испарения или кипения.
Испарением называется парообразование, происходящее только с поверхности жидкости. Этот процесс про
Hs-ДИАГРАММА ВОДЯНОГО ПАРА
В инженерной практике термодинамические процессы с водяным паром рассчитывают с помощью hs-диаграммы. Эта диаграмма в СССР построена до давления 100,0 МПа и до температуры 1000
ПАРАМЕТРЫ ВОДЫ И ВОДЯНОГО ПАРА
При исследованиях принято считать, что при 0 0С и любом давлении энтальпия h0, внутренняя энергия u0, энтропия s0 воды равны нулю. В изоб
ЦИКЛ КАРНО ДЛЯ ВОДЯНОГО ПАРА
Наиболее совершенным идеальным циклом паросиловой установки является прямой обратимый цикл Карно, термический КПД которого, как отмечалось выше, максимальный в заданном интервале температур и не за
ЦИКЛ РЕНКИНА
Основным идеальным циклом паросиловых установок является цикл Ренкина. На рисунке 24 приведена принципиальная схема паросиловой установки, работающей по циклу Ренкина, а на рисунке 25 – rJ- и Ts-ди
ЦИКЛА РЕНКИНА
Исследование выражения для термического КПД цикла Ренкина при различных начальных (на входе в паровую турбину) и конечных (на входе в конденсатор) параметрах пара позволяет сделать вывод – начально
ВЛАЖНЫЙ ВОЗДУХ
В качестве рабочего тела атмосферный воздух применяется при сушке, нагреве, охлаждении различных материалов, в установках кондиционирования и т. д.
В атмосферном воздухе со
ВЛАЖНОГО ВОЗДУХА
Согласно закону Дальтона, давление смеси газов равно сумме парциальных давлений ее компонентов:
pнл.в. = pс.в. + pв.п., (128)
&nbs
Hd-ДИАГРАММА ВЛАЖНОГО ВОЗДУХА
Данная диаграмма позволяет наиболее просто и быстро определять параметры влажного воздуха.
В Hd-диаграмме (рис. 27, а) по оси абсцисс откладывается влагосодержание d (г/кг сухого воздуха),
ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ
Одно из основных понятий теплопроводности – температурное поле. Температура – один из основных параметров, характеризующих тепловое состояние рабочего тела или среды. Совокуп
ЗАКОН ФУРЬЕ
Закон Фурье устанавливает количественную взаимосвязь между температурным полем и интенсивностью распространения теплоты в нем посредством теплопроводности. Согласно закону Фурье, ве
ПРИ СТАЦИОНАРНОМ РЕЖИМЕ
Теплопроводность однослойной плоской стенки. Схема распространения теплоты для этого случая приведена на рисунке 30. Пусть теплота распространяется в стенке, ограниченной пар
КОНВЕКТИВНОГО ТЕПЛООБМЕНА
В практике наиболее часто приходится рассчитывать конвективный теплообмен между жидкостью (газом) и поверхностью твердого тела или канала (трубы), по которому она протекает. Если пр
ПРИ КИПЕНИИ ЖИДКОСТИ
Теплоотдача при кипении жидкости сопровождается изменением агрегатного состояния рабочего тела. Это явление имеет специфические особенности и большое практическое значение для энерг
И ЗАКОНЫ ИЗЛУЧЕНИЯ
Теплообмен излучением – процесс переноса теплоты в виде электромагнитных волн (фотонов). Этот вид теплообмена осуществляется в три этапа: внутренняя энергия тела в начале пре
ТЕПЛООБМЕНА ИЗЛУЧЕНИЕМ
Знание законов излучения позволяет получить расчетные формулы для лучистого теплообмена между телами. В частности, формулой (155) пользуются при определении излучательной способност
ТЕПЛОПЕРЕДАЧА. СНОВЫ РАСЧЕТА ТЕПЛООБМЕННЫХ АППАРАТОВ
Разделение процесса переноса теплоты на теплопроводность, конвективный теплообмен и теплообмен излучением удобно для его изучения. В действительности встречается сложный теплообмен,
ТЕПЛОПЕРЕДАЧА ЧЕРЕЗ ПЛОСКУЮ СТЕНКУ
Пусть однослойная плоская стенка (рис. 37) толщиной d из материала, коэффициент теплопроводности которого l, омывается с одной стороны горячей жидкостью с температурой tж1
ТЕПЛОПЕРЕДАЧА ЧЕРЕЗ ЦИЛИНДРИЧЕСКУЮ СТЕНКУ
В практике наиболее распространенным элементом теплообменных устройств является труба. Схема процесса теплопередачи через цилиндрическую стенку (трубу) представлена на рисунке 38.
ТЕПЛОВАЯ ИЗОЛЯЦИЯ
При решении практических задач теплопередачи требуется либо повысить интенсивность переноса теплоты от греющей среды к нагреваемой, либо, наоборот, затормозить этот процесс. Интенси
ТЕПЛООБМЕННЫЕ АППАРАТЫ
Теплообменными аппаратами (теплообменниками) называются устройства, предназначенные для передачи теплоты от греющего теплоносителя (с более высокой температурой) к нагреваемому тепл
ЭНЕРГЕТИЧЕСКОЕ ТОПЛИВО
Энергетическим топливом называют такие горючие вещества, которые экономически целесообразны при сжигании в технических устройствах для получения теплоты.
В качестве топлива
ПОНЯТИЕ УСЛОВНОГО ТОПЛИВА
Теплота сгорания топлива показывает, какое количество теплоты (в килоджоулях) выделяется при полном сгорании твердого, жидкого или газообразного топлива при нормальных условиях.
ОСНОВНЫХ КОМПОНЕНТОВ ТОПЛИВА
Главная составляющая горючей части топлива – углерод. Теплота сгорания углерода – 33 650 кДж/кг. Содержание углерода по горючей массе топлива составляет: в антраците – 87…93%
ВИДОВ ТОПЛИВА
Древесина. Использование древесины в качестве топлива ограничено. Теплота сгорания дров в значительной степени определяется влажностью. Чем больше влажность дров, тем меньше
СУЩНОСТЬ ПРОЦЕССА ГОРЕНИЯ ТОПЛИВА
В зависимости от скорости горения различают нормальное горение и взрывное. Скоростью горения называется скорость распространения пламени. При нормальном горении скорость распростран
ДЛЯ ПОЛНОГО СГОРАНИЯ ТОПЛИВА
Если состав топлива известен, то количество воздуха, необходимого для полного сгорания любого из его компонентов, можно определить из выражения С + О2 = СО2. Э
ОБЪЕМ И СОСТАВ ПРОДУКТОВ СГОРАНИЯ
Для правильного расчета и выбора теплотехнических агрегатов необходимо знать количество образующихся продуктов сгорания. Как правило, количество продуктов сгорания относят к 1 кг тв
Численные значения энтальпий составляющих продуктов сгорания и воздуха при различных температурах
Температура,
К
НСО2, кДж/м3
НN2, кДж/м3
НО2,
кДж/м3
УКАЗАТЕЛЬ ЛИТЕРАТУРЫ
Алексеев Г. Н. Общая теплотехника.– М.: Высшая школа, 1980. Андрющенко А. И. Основы термодинамики циклов теплоэнергетических установок.– М., Высшая школа. Ар
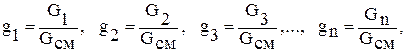
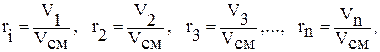 (19)
(19)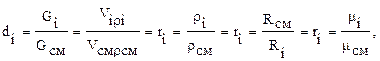 (20)
(20)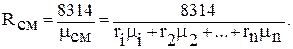 (21)
(21)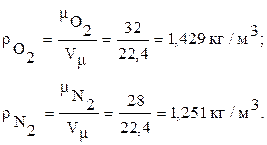
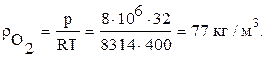







Новости и инфо для студентов