рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- Понятие о сплавах
Реферат Курсовая Конспект
Понятие о сплавах
Понятие о сплавах - раздел Химия, Реальное строение металлических кристаллов Сплав – Это Вещество, Полученное Сплавлением, Спеканием, Электролизом, Возгон...
Сплав – это вещество, полученное сплавлением, спеканием, электролизом, возгонкой двух или более элементов. Сплав, приготовленный из металлов или имеющий металлическую основу и обладающий металлическими свойствами называется металлическим сплавом (МС). МС более сложное вещество, чем чистый металл, МС обладают более высокими прочностными и другими механическими свойствами по сравнению с чистыми металлами. Им часто придаются специфические свойства. Поэтому они получили более широкое применение.
Характер взаимодействия компонентов в сплавах зависит от их положения в таблице Менделеева, особенностей строения атомов, их электронных оболочек, типов и параметров решёток, соотношения температур плавления, их атомных диаметров, растворимости друг в друге и других факторов. МС может быть: а) механической смесью, б) химическим соединением, в) раствором элементов друг в друге с неограниченной или ограниченной растворимостью, а также их промежуточными смесями.
Механическая смесь двух и более компонентов возможна тогда, когда металлы (вещества, элементы) не растворимы в твёрдом состоянии и не вступают в химическую реакцию с образованием соединений. Рентгенограмма показывает наличие двух решёток компонентов А и Б, что соответствует чистым металлам. Механические свойства соответствуют и зависят от количества компонентов А и Б.
Химическое соединение (ХС). При образовании ХС достигается следующее:
- соотношение атомов элементов соответствует стехиометрической пропорции Аm × Вn ;
- образуется новая отличная от элементов кристаллическая решётка с упорядоченным расположением атомов;
- ХС характеризуется определёнными физическими свойствами (температура плавления, удельный вес, электро- и теплопроводность, мехсвойства, запах, вкус, ковкость, пластичность и т.д.).
Если ХС образуется металлами, то в углах решётки располагаются атомы (ионы), между ними электронный газ. К таким элементам относятся Cu2MnSn, CuAl2, CuAu, CuAg и т.п. Связи жёсткие, химические соединения образуются без учёта валентности.
При образовании химсоединения металла с неметаллом возникает ионная связь. Элементы удерживаются электронным притяжением (NaCl, KMnO4 и т.д.)
В жидком состоянии большинство металлических сплавов представляют однородные жидкие растворы. При переходе в твёрдое состояние однородность сохраняется, сохраняется и растворимость. Рентгеновский анализ обнаруживает только один тип решётки. В отличие от механических смесей твёрдый раствор является однофазным. В отличие от химического соединения твёрдый раствор существует не при строго определённом соотношении компонентов, а в интервале концентрации. Различают твёрдые растворы замещения и внедрения. Замещают металлы друг друга, заменяя в узлах решётки. Внедряются в металл обычно элементы с малым диаметром атома (C, H, N и др.). С образованием твёрдых растворов внедрения периоды решётки увеличиваются.
Замечено, что неограниченная растворимость наблюдается у элементов относительно близко расположенных друг от друга в периодической системе. Если элементы расположены друг от друга далеко и имеют различную физическую природу, то они чаще всего склонны к образованию химических соединений, а не твёрдых растворов.
Химические соединения могут также образовывать растворы замещения, растворять другие атомы. Например, борид железа (Fe4B2) способен растворять хром, углерод.
Электронные соединения могут образовывать металлы следующих групп: Cu, Ag, Au, Fe, Co, Ni, Pt, Pd, Be, Zn, Cd, Al, Sn, Si
Электронные соединения встречаются в важнейших сплавах: Cu-Zn; Cu-Sn; Fe-Al; Cu-Si; Al-Si; Cu-Al и т.д. Обычно в системе наблюдаются три фазы (β, γ, ε). Электронные соединения промежуточные между хим. соединениями и твёрдым раствором.
Диаграммы состояния представляют собой графическое изображение фаз и структур в зависимости от температуры, давления и концентрации элементов.
Фаза – это однородная часть системы, отделённая от других частей системы (фаз) поверхностью раздела, при переходе через которую изменяется состав, часто решётка, структура скачкообразно.
Компоненты – вещества, образующие систему.
Состояние одного компонента – прямая линия; диаграмма состояния 2-х компонентов системы – плоская фигура (на оси ординат откладывается t 0С, на оси абсцисс – концентрация элементов); 3-х компонентная система – пространственная фигура с основанием в виде треугольника и т.д.
Линия начала кристаллизации называется точкой ликвидуса, конец кристаллизации – точка солидуса.
Имеются следующие диаграммы:
а) диаграмма состояния 1-го рода описывает 2-х компонентную систему, где компоненты нерастворимы друг в друге (рис. 22). Сплав с минимальной температурой плавления (точка С) называется эвтектикой, температура – эвтектической. Количество компонентов находят по правилу отрезков: линия 1 - s определяет всё количество сплава, t - s - количество оставшейся жидкости  ; линия 1 - t - количество кристаллов
; линия 1 - t - количество кристаллов  .
.
В доэвтектических сплавах содержится компонент А совместно с эвтектикой (АВ), в заэвтектических содержится компонент В с эвтектикой (АВ).
б) диаграмма состояния 2-го рода описывает сплавы с неограниченной растворимостью в жидком и твёрдом состоянии (рис 23). Выше АСВ находится область жидкой фазы (ж); между АСВ и АDВ расположена двухфазная область ( +ж), ниже АDВ -
+ж), ниже АDВ -  - фаза.
- фаза.

а б
а – диаграмма состояния; б – схемы получающихся структур
Рисунок 22 – Диаграмма состояния I рода и схемы получающихся структур

а б
а – кривые охлаждения; б – диаграмма состояния
Рисунок 23 – Диаграмма состояния для случая неограниченной растворимости компонентов А и В в твёрдом и жидком состоянии
в) диаграмма состояния 3-го рода описывает сплавы с ограниченной растворимостью в твёрдом состоянии, не образующих химическое соединение. На рисунке 24 изображена диаграмма с эвтектикой, на рисунке 25 – с перитектикой. Перитектическая реакция ж+ .
.

а б
а – кривые охлаждения; б – диаграмма состояния
Рисунок 24– Кривые охлаждения и диаграмма состояния сплавов, образующих ограниченные твердые растворы и эвтектику

Рисунок 25 – Диаграмма состояния сплавов, образующих ограниченные твердые растворы и испытывающих перитектическое превращение
Ограниченная растворимость наиболее часто встречается в металлических сплавах. Линия а-с-в ликвидус, линия a-d-c-e-в – солидус. Выше “acв” расположена жидкость, между “асв” и “adceв” – жидкость и кристаллы  - фазы, жидкость и кристаллы
- фазы, жидкость и кристаллы  - фазы. В точке С образуется эвтектика – сплав
- фазы. В точке С образуется эвтектика – сплав  и
и  фаз с самой низкой температурой плавления. Ниже “adcев” находятся твёрдые фазы. В области a-d-f находится
фаз с самой низкой температурой плавления. Ниже “adcев” находятся твёрдые фазы. В области a-d-f находится  фаза в твёрдом состоянии. Точка d характеризует предельную (максимальную) растворимость компонента B в А при температуре образования эвтектики. Линия “d-f” – характеризует изменение концентрации компонента B в А в зависимости от изменения температуры точки “e”
фаза в твёрдом состоянии. Точка d характеризует предельную (максимальную) растворимость компонента B в А при температуре образования эвтектики. Линия “d-f” – характеризует изменение концентрации компонента B в А в зависимости от изменения температуры точки “e”
Правее лини “в-e-к” находится  - фаза, между линиями с-В и в-В находится кристаллизующийся расплав жидкость и
- фаза, между линиями с-В и в-В находится кристаллизующийся расплав жидкость и  - фаза, линия “е-к” показывает изменение концентрации элемента А в В. В точке “e” максимальная концентрация элемента А в В при температуре образования эвтектики. Под линией “d-f” при медленном охлаждении образуется смесь
- фаза, линия “е-к” показывает изменение концентрации элемента А в В. В точке “e” максимальная концентрация элемента А в В при температуре образования эвтектики. Под линией “d-f” при медленном охлаждении образуется смесь  2- фаз.
2- фаз.  2- два ставится потому, что первичные кристаллы
2- два ставится потому, что первичные кристаллы  выпадают из жидкости, а из
выпадают из жидкости, а из  - фазы при понижении температуры и уменьшении растворимости выпадают вторичные кристаллы (
- фазы при понижении температуры и уменьшении растворимости выпадают вторичные кристаллы ( 2). То же происходит справа: в точке “e” максимальная растворимость А в В, при понижении температуры растворимость компонента А в В изменяется по кривой е-к, под линией “е-к” находится сплав, состоящий из
2). То же происходит справа: в точке “e” максимальная растворимость А в В, при понижении температуры растворимость компонента А в В изменяется по кривой е-к, под линией “е-к” находится сплав, состоящий из  +
+ 2. Под линией “d-c” расположен раствор эвтектика +
2. Под линией “d-c” расположен раствор эвтектика + +
+ 2 , под линией “с-в” - эвтектика +b+α2.
2 , под линией “с-в” - эвтектика +b+α2.
Разберем пример сплава 1. Сплав 1 между точками t1 - t2 состоит из жидкости и  - фазы, между t2 – t3 имеется одна фаза
- фазы, между t2 – t3 имеется одна фаза  , между t3 и t0 раствор состоит из
, между t3 и t0 раствор состоит из  фазы и
фазы и  2, которая выпадает и
2, которая выпадает и  - фазы, так как уменьшается растворимость
- фазы, так как уменьшается растворимость  в
в  при понижении температуры. Если сплав (
при понижении температуры. Если сплав ( и
и  2) вновь нагреть до температуры выше t3 , то
2) вновь нагреть до температуры выше t3 , то  2 растворится в
2 растворится в  - фазе. Если очень быстро охладить
- фазе. Если очень быстро охладить  - фазу, то
- фазу, то  2 не сможет выделиться и получится пересыщенный раствор
2 не сможет выделиться и получится пересыщенный раствор  2 в
2 в  фазе. Этот процесс называется закалкой. Пересыщенный раствор неустойчив, нестабилен, прочен, твёрд, а при нагреве (а иногда при температуре ~ 20 0С) начинает распадаться с выделением дисперсных частиц избыточной фазы
фазе. Этот процесс называется закалкой. Пересыщенный раствор неустойчив, нестабилен, прочен, твёрд, а при нагреве (а иногда при температуре ~ 20 0С) начинает распадаться с выделением дисперсных частиц избыточной фазы  2. Распад пересыщенного твёрдого раствора, полученного при закалке, называется старением для цветных металлов и отпуском для чёрных металлов, если их нагревают до определённых температур. Выделение упрочняющей фазы (
2. Распад пересыщенного твёрдого раствора, полученного при закалке, называется старением для цветных металлов и отпуском для чёрных металлов, если их нагревают до определённых температур. Выделение упрочняющей фазы ( 2) сопровождается разупрочнением сплава. Термическая обработка, вызывающая полное выделение упрочняющей фазы и разупрочнение, называется отжигом. Избыточная фаза
2) сопровождается разупрочнением сплава. Термическая обработка, вызывающая полное выделение упрочняющей фазы и разупрочнение, называется отжигом. Избыточная фаза  2 чаще всего бывает химическим соединением. Правее линии “е-к” происходят подобные процессы, но получают пересыщенный раствор
2 чаще всего бывает химическим соединением. Правее линии “е-к” происходят подобные процессы, но получают пересыщенный раствор  2 в
2 в  - фазе. Эвтектические сплавы хорошо льются, т.к. имеют самую низкую температуру плавления, но хуже обрабатываются давлением.
- фазе. Эвтектические сплавы хорошо льются, т.к. имеют самую низкую температуру плавления, но хуже обрабатываются давлением.
Сплавы, расположенные левее точки d однофазные и лучше обрабатываются давлением, хуже льются.
При кристаллизации часто наблюдается разность химсостава по сечению литой заготовки. Этот процесс называется ликвацией.
Разберём коротко диаграмму с перетектикой (рис.25). Точка d характеризует максимальную растворимость компонента B в A, а точка “e”- предельную растворимость A в B. Линия “CDE” – линия перетектического превращения. При эвтектическом превращении кристаллизуется сразу 2 фазы, при перетектическом превращении кристаллизуется одна фаза из ранее выпавшей твёрдой фазы и жидкости. Из жидкого раствора правее точки d из жидкой фазы в начале выделяется  фаза. При достижении температуры tn в равновесии находится жидкость и
фаза. При достижении температуры tn в равновесии находится жидкость и  кристаллы состава точки “e”.
кристаллы состава точки “e”.  - кристаллы образуются при перетектической реакции
- кристаллы образуются при перетектической реакции  е+жс+
е+жс+ е
е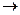
 d.
d.
Неизрасходованная часть жидкости и кристаллы  превращаются жс+
превращаются жс+ е
е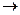
 d+
d+ е
е
Кристаллизация сплавов по “c-d” происходит по формуле жс+ е
е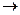 жс+
жс+ d
d
г) диаграмма состояния сплава, образующего устойчивое химическое соединение (рис. 26) Аm × Вn. Устойчивых соединений может быть 1,2,3…

Рисунок 26 – Диаграмма состояния IV рода
д) диаграмма состояния с неустойчивым химическим соединением представлена на рисунке 27. На линии d-c-t в равновесии находится три фазы: Жд+кристаллы компонента В и кристаллы химсоединения An Bm. Выше линии DCF происходит An Bm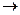 L+B, ниже происходит реакция LД +В
L+B, ниже происходит реакция LД +В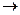 An Bm.
An Bm.

Рисунок 27 – Диаграмма состояния с неустойчивым химическим соединением
е) диаграмма состояния для сплавов, испытывающих полиморфные (аллотропические) превращения показана на рисунке 28. В приведённых выше диаграммах рассматривалась первичная и вторичная кристаллизации, закалка. Вторичная кристаллизация происходит, если хотя бы один компонент претерпевает аллотропические (полиморфные) превращения (Fe, Mn, Co, Ti, Sn, и некоторые другие). В диаграммах а-б-в-г на рисунке 28 в верхней части происходит первичная кристаллизация, в нижней вторичная. В диаграмме “a” закалка возможна в зоне С-Д-Р, т.к. находится 2 фазы. В диаграмме “б” две фазы находится в области CDF, в диаграмме “в” упрочнение происходит в области, где одновременно присутствует 2 фазы ( +
+ ). На диаграмме “г” при температуре С-Е-Д происходит выделение
). На диаграмме “г” при температуре С-Е-Д происходит выделение  1 и
1 и  2 фаз и
2 фаз и  фазы –
фазы – 
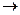
 1 +
1 + 2.
2.

Рисунок 28 – Диаграммы состояния с полиморфными превращениями
Перечисленные выше диаграммы равновесные, т.е. выполнены при малых скоростях охлаждения. Изучив теоретическую кристаллизацию, можно рассматривать неравновесные условия, когда могут не происходить диффузионные процессы при различных переохлаждениях.
В реальных условиях первые кристаллы имеют большую концентрацию тугоплавкого компонента. Последующие кристаллы самые легкоплавкие. Это явление называется ликвацией. Она может быть уменьшена длительным диффузным отжигом или обработкой давлением.
Неравновесная кристаллизация происходит при большом переохлаждении. Чем больше переохлаждение, тем мельче будут вторичные кристаллы, тем напряжённей и неустойчивее система. Получается пересыщенный раствор одного компонента в другом – мартенсит, который прочен, твёрд. Этот процесс называется закалкой. Нагревая сплав после закалки, мы приводим систему в более устойчивое состояние, снижая прочность. Этот процесс называется отпуском или старением. С помощью термообработки можно изменять механические свойства сплавов.
2.2 Диаграмма железо – углерод
Железоуглеродистые сплавы (стали, чугуны) важнейшие, так как их производят 90-95% от общего производства всех металлов. Начало изучению диаграммы положено Д.К.Черновым, П.П.Амосовым. Было указано о существовании критических точек в стали, дано первое представление о диаграмме Fe-С. Зарубежные учёные Осмонд, Ле – Шателье, Аустенит, русские – Байков, Гудцов, Гуляев развивали науку о диаграмме Fe-С.
Железо плавится при 1539 0С. В твёрдом состоянии оно имеет три решётки a (ОЦК), g (ГЦК) и a1 (ОЦК). Fea существует до 911 0С, Feg - от 911 до 1392 0С, Fea1 - 1392-1539 0С. Техническое железо имеет относительно низкую прочность sв – 20 25
25  ; sт – 10-12
; sт – 10-12  ; НВ – 80-70
; НВ – 80-70  и высокие пластичные y и d свойства 80% и 50%.
и высокие пластичные y и d свойства 80% и 50%.
При 768 0С и выше железо становится немагнитным. Железо со многими элементами образует сплавы (растворы):
а) с металлами – растворы замещения, с Fe3C также раствор замещения;
б) с лёгкими элементами – растворы внедрения (C, B, N, и др.).
Растворимость углерода в железе зависит от его кристаллической решётки. В Fea растворится от 0,005% (20 0С) до 0,02% (723 0С), в Feg растворится максимально 2,14% углерода.
В ОЦК решётке (Fea) имеется 12 свободных мест в середине рёбер. Свободное место (пора) имеет размер 0,62 А0. Диаметр атома углерода 1,54 А0. Такой размер недостаточен для помещения в него атома углерода. В Feg (ГЦК) решётке в центре имеется пора диаметром 1,02 А0. В этой поре помещается атом углерода, увеличивая размер g - железа.
Твёрдый раствор внедрения углерода и других элементов в a - железо называется ферритом (рис. 29), а в g железо – аустенитом (рис. 30).

Рисунок 29 – Микроструктура технического железа. Феррит

Рисунок 30 –Структура аустенита углеродистой стали, выявленная травлением при высоких температурах
Цементит (Ц, Fe3C) – это химическое соединение углерода с железом (карбид железа), имеющий свою решётку, физико-химические свойства (рис 31). Температура плавления ~ 1500 0С, не полиморфен, слабо магнитен. Он имеет высокую твёрдость (80 HRС), низкую пластичность. Цементит с железом и другими металлами образует твёрдые растворы замещения. Углерод может замещаться азотом, кислородом, бором и др., атомы железа металлами: Mn, Cr, W, Ni, Co, Cu и т.д. Такой твёрдый раствор на базе решётки цементита и железа называется легированным.

Рисунок 31 – Кристаллическая структура цементита
Диаграмма Fe – C изображена на рисунке 32.

Рисунок 32 – Диаграмма фазового состояния Fe-Fe3C
Линия ABCД – ликвидус, AHJECF – солидус. В системе существуют следующие фазы:
- жидкий сплав (раствор) углерода в железе обозначается Ж или Z;
- цементит (Fe3C) линия ДFKL (Ц);
- феррит (Fea, Ф, a) расположен в областях GPQ и AHN;
- аустенит (Feg, А, g) занимает область NJESG.
На диаграмме имеется три горизонтальные линии HJB, ECF, PSK указывающие на протекание трёх реакций. При 1499 0С ЖB+ФН ®АJ; реакция протекает у сплавов, содержащих углерод от 0,1 до 0,5 %. Реакция – перитектическая. При 1147 0С протекает эвтектическая реакция ЖС ®AE +ЦF в результате образуется механическая смесь аустенита и цементита – эвтектика – ледебурит. Реакция протекает у всех сплавов, содержащих углерод более 2,14%. При температуре меньше 727 0С ледебурит состоит из перлита и цементита.
При 727 0С протекает эвтектоидная реакция AS ®ФР +ЦК. Продуктом её является механическая смесь феррита и цементита вторичного – перлит (рис. 33). Перлитное превращение происходит у всех сплавов, содержащих углерод более 0,02%.

Рисунок 33 – Структура перлита
Диаграмма Fe – Fe3C – метастабильная. Концентрация углерода для характерных точек следующая: B – 0,51 %C, H – 0,1 %C, J – 0,16 %C, E – 2,14 %C, C – 4,3 %C, S – 0,8 %C, P – 0,02 %C.
В системе Fe – Fe3C имеются сплавы: сталь и чугун. Стали содержат углерод до 2,14 %, чугуны от 2,14 до 6,67 %, сталь, содержащая 0,8 % углерода называется эвтектоидной, чисто перлитной. Стали доэвтектоидные (конструкционные) содержат до 0,8 % углерода; стали, содержащие углерод от более 0,8 до 2,14 называются заэвтектоидными (инструментальными). На рисунке 34 показана доэвтектоидная (Ф+П), эвтектоидная (П) и заэвтектоидная (П+Ц2) стали. Перлит имеет кристаллы феррита вперемешку с кристаллами цементита.

а б в
а – доэвтектоидная сталь;
б – эвтектоидная сталь;
в – заэвтектоидная сталь
Рисунок 34 – Микроструктура сталей
Чугун, содержащий углерода больше 2,14%, но меньше 4,3% называется доэвтектическим (конструкционным), 4,3% - эвтектическим, а при содержании углерода более 4,3 но менее 6,67 – заэвтектическим. На рисунке 35 изображены названные чугуны. Доэвтектический чугун (рис. 35 а) содержит структуру П+Л (П+Ц2)+Ц2, эвтектический чугун (рис. 35 б) содержит ледебурит (П+Ц). Заэвтектический чугун (рис. 35 в) содержит Л (П+Ц)+Ц1.

а б в
а – доэвтектический чугун;
б – эвтектический чугун;
в – заэвтектический чугун
Рисунок 35 –Микроструктура чугунов
– Конец работы –
Эта тема принадлежит разделу:
Реальное строение металлических кристаллов
Содержание... Введение Основы теории сплавов Классификация...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Понятие о сплавах
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов