рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- Завдання для самостійної роботи
Реферат Курсовая Конспект
Завдання для самостійної роботи
Завдання для самостійної роботи - раздел Химия, Техніка безпеки в хімічній лабораторії . Розрахуйте Стандартний Тепловий Ефект Реакц...
.
Розрахуйте стандартний тепловий ефект реакцій і зробіть висновок: як вони протікають з виділенням або поглинання тепла?
1) 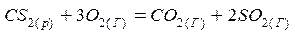 ;
;
2) 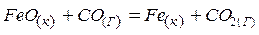 ;
;
3) 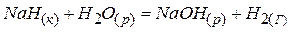 ;
;
4) 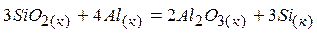 .
.
Самостійно вирішити задачі № 283, 288, 300, 303, 311 [5. с. 75-78]
Таблиця 2. ТЕРМОДИНАМІЧНІ КОНСТАНТИ ДЕЯКИХ СПОЛУК
| Сполука | Агрегатний стан | 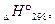 кДж/моль кДж/моль
| 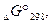 кДж/моль
кДж/моль
| 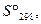 Дж/(моль К)
Дж/(моль К)
| Сполука | Агрегатний стан | 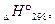 кДж/моль кДж/моль
| 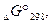 кДж/моль
кДж/моль
| 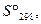 Дж/(моль К)
Дж/(моль К)
|
| AI | к | 42,7 | KCl | к | -435,9 | -408,0 | 82,6 | ||
| AI2О3 | к | -1669,8 | -1582,0 | 50,9 | КНSO4 | к | -1158,1 | -1043,5 | 187,9 |
| Al2(SО4)3 | к | -3434 | -3091,9 | 239,2 | К2SO4 | к | -1433,4 | -1316,4 | 175,7 |
| ВаО | к | -556,6 | -528,4 | 70,3 | КNO3 | к | -492,7 | -393,1 | 133,0 |
| ВаСОз | к | -1202,0 | -1138,8 | 112,1 | MgO | к | -601,2 | -569,6 | 26,9 |
| ВеО | к | -598,7 | -581,6 | 14,1 | MgCO3 | к | -1096,2 | -1029,3 | 65,7 |
| ВеСОз | к | -981,6 | -944,8 | 199,4 | N2 | г | 191,5 | ||
| С(графіт) | к | 5,7 | NH3 | г | -46,2 | -16,7 | 192,5 | ||
| СаО | к | -635,5 | 604,2 | 39,7 | NH4NO3 | к | -365,4 | -183,8 | |
| СаСО3 | к | -1207,0 | -1127,7 | 88,7 | NH4Cl | к | -315,4 | -203,7 | 94,5 |
| Са (ОH)2 | к | -986,2 | -896,76 | 83,4 | NO | г | +90,4 | +86,7 | 210,2 |
| Са3 (PО4)2 | г | -4125,0 | -3899,5 | 240,9 | N2O | г | +81,6 | +103,6 | 220,0 |
| СО | г | -110,5 | -137,3 | 197,9 | NO2 | г | +33,5 | +51,5 | 240,2 |
| CO2 | г | -393,5 | -394,4 | 213,6 | N2O4 | г | +94,0 | +98,3 | 304,3 |
| СОСl2 | г | -220,3 | -266,9 | 283,9 | N2O3 | г | +83,8 | +307,0 | 140,5 |
| СН4 | г | -74,8 | -50,7 | 186,2 | NaH | к | -57,0 | - | - |
| С2Н6 | г | -82,9 | -32,9 | 229,5 | NaOH | к | -469,5 | -377,0 | 64,2 |
| С6Н6 | p | +49 | +124,5 | 173,2 | NaCl | к | -410,9 | -384 | 72,4 |
| С2Н2 | г | +226,8 | +209,2 | 200,8 | NaF | к | - | -541,0 | - |
| С2Н4 | г | +52,3 | +68,1 | 219,4 | Ni | к | 29,87 | ||
| СН3ОН | p | -238,7 | -166,3 | 126,8 | NiO | к | -239,7 | -211,6 | 38,0 |
| C2H5OH | p | -227,6 | -174,8 | 160,7 | O2 | г | 205,0 | ||
| C2H5OH | г | -235,3 | - | - | PH3 | г | +5,4 | +13,4 | 210,23 |
| С6Н12О6 | к | -1273,0 | -919,5 | - | P2O5 | к | -1492,0 | -1348,8 | 114,5 |
| СS2 | p | +115,3 | +65,1 | 237,8 | POCl3 | p | -597,1 | -521,3 | 222,5 |
| Сl2 | г | 222,9 | PCl5 | г | -277 | -286,3 | 352,7 | ||
| Cu | к | 33,3 | PCl3 | г | -369,4 | -324,6 | 311,6 | ||
| CuO | к | -162,1 | -129,9 | 42,6 | Pb | к | 64,9 | ||
| Cu(NO3) 2 | к | -307,11 | -114,22 | 193,3 | PbO | к | -219,3 | -189,1 | 66,1 |
| Сг2О3 | к | -1141,0 | -1046,8 | 81,1 | PbO2 | к | -276,6 | -219 | 76,4 |
| Fe | к | 27,2 | PbCl2 | к | -359,8 | 82,6 | -408,0 | ||
| FeO | к | -264,8 | -244,3 | 60,8 | S(ромб) | к | 31,9 | ||
| Fe2O3 | к | -822,1 | -740,3 | 87,4 | SO2 | г | -296,9 | -300,2 | 248,1 |
| Fe3O4 | к | -1117,1 | -1014,2 | 146,2 | SO3 | г | -395,2 | -370,4 | 256,2 |
| H2 | г | 130,6 | Si | к | 18,8 | ||||
| H2O | г | -241,8 | -238,6 | 188,7 | SiO2 | к | -910,9 | -856,7 | 41,8 |
| H2O | p | -285,8 | -237,2 | 69,9 | SnO2 | к | -580,8 | -519,65 | 52,3 |
| H2O2 | p | -187,4 | -117,6 | 105,9 | SrO | к | -590,4 | -559,8 | 54,4 |
| HCl | г | -92,3 | -95,2 | 186,7 | SrCO3 | к | -1221,3 | -1137,6 | 97,1 |
| H2S | г | -20,2 | -33,8 | 205,6 | Ti | к | 30,7 | ||
| H2SO4 | p | -811,3 | -742,0 | 156,9 | TiO2 | к | -943,9 | -888,5 | 50,3 |
| Hg | к | 76,1 | Zn | к | 41,63 | ||||
| Hg2Cl2 | к | -264,8 | -210,7 | 195,8 | ZnO | к | -350,6 | -320,7 | 43,6 |
| HgCl2 | к | -230,1 | -185,8 | 144,4 |
Виконайте експеримент та заповніть лабораторний журнал:
Дотримуйтесь правил техніки безпеки! (стор.5)
Питома вага розчинів: 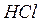
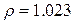 г/мл;
г/мл; 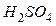
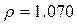 г/мл;
г/мл; 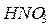
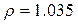 г/мл;
г/мл; 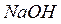
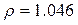 г/мл;
г/мл; 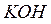
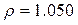 г/мл.
г/мл.
| № | Зміст роботи | Рівняння реакцій, спостереження, розрахунки | |||
З бюреток відміряйте у стаканчики по 25 мл розчинів:
· У один стаканчик з бюретки налийте 25 мл розчину кислоти, а у другий – 25 мл розчину лугу.
· Вставте воронку в боковий отвір внутрішньої посудини калориметра та обережно перелийте в нього із стаканчика розчин кислоти.
· Запишіть температуру розчину кислоти з точністю до 0,10 (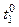 ).
· Влийте за допомогою воронки у калориметр розчин лугу.
· Обережно та старанно перемішайте мішалкою розчин. Слідкуйте за підвищенням температури до тих пір, поки вона не почне падати.
· Запишіть максимальну температуру розчину ( ).
· Влийте за допомогою воронки у калориметр розчин лугу.
· Обережно та старанно перемішайте мішалкою розчин. Слідкуйте за підвищенням температури до тих пір, поки вона не почне падати.
· Запишіть максимальну температуру розчину (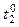 ). ).
|
Рівняння реакції:
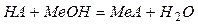 ; ;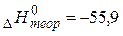 кДж/моль кДж/моль
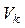 - (об’єм кислоти) =______мл - (об’єм кислоти) =______мл
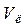 - (об’єм лугу) =_________мл - (об’єм лугу) =_________мл
 - питома вага розчину кислоти =______г/мл - питома вага розчину кислоти =______г/мл
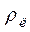 - питома вага розчину лугу = ________ г/мл - питома вага розчину лугу = ________ г/мл
| ||||
| Розрахуйте маси кислоти, лугу та масу всього розчину |
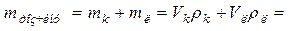 ______мл ______мл
| ||||
| Обчисліть кількість тепла (q) | 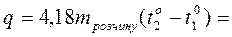 ______Дж ______Дж
| ||||
| Перерахуйте теплоту q на 1 еквівалентну масу кислоти | 1. Знаходимо кількість 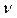 еквівалентів у 25 мл розчину еквівалентів у 25 мл розчину
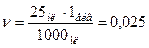 еквівалентів
2. еквівалентів
2. 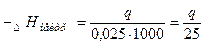 (кДж) (кДж)
| ||||
Розрахуйте відносну похибку визначення теплоти реакції нейтралізації 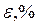
| 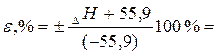 ______% ______%
| ||||
Висновки і місце для домашніх задач:
Оцінка__________ Дата___________ Підпис викладача____________
– Конец работы –
Эта тема принадлежит разделу:
Техніка безпеки в хімічній лабораторії
СХІДНОУКРАЇНСЬКИЙ НАЦІОНАЛЬНИЙ УНІВЕРСИТЕТ імені ВОЛОДИМИРА ДАЛЯ... ЛАБОРАТОРНИЙ ЖУРНАЛ...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Завдання для самостійної роботи
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов