рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Механика
- /
- Вид работы: Конспекты Лекций
- /
- Кинетика активной среды кислородно-йодного лазера
Реферат Курсовая Конспект
Кинетика активной среды кислородно-йодного лазера
Кинетика активной среды кислородно-йодного лазера - Конспект Лекций, раздел Механика, Термодинамика. Конспект лекций Закон Действующих Масс Константа Скорости Реакции Сечение...
Закон действующих масс
Константа скорости реакции
Сечение реакции
Пусть в смеси газов идет реакция, в результате которой одни компоненты смеси преобразуются в другие. Это может быть как истинно химическая реакция, то есть процесс перестройки структуры химических связей, так и другие процессы преобразования, например – электронный обмен, колебательный или вращательный обмен. Под этим понимаются процессы обмена энергией, приводящие к изменениям в квантовом состоянии атомов и молекул. Эти процессы, также как и истинно химические реакции, происходят при столкновениях, что позволяет формально считать их химическими реакциями и описывать с ними единым образом.
В основе описания кинетики любой реакции лежит закон действующих масс, согласно которому скорость реакции пропорциональна произведению концентраций реагентов. Разберемся в смысле этих понятий.
Реакция происходит (с какой-то вероятностью, меньшей единицы) при столкновении молекул (атомов) реагентов. Скорость реакции – это количество актов реакции, происходящее в единице объема среды в единицу времени. Размерность скорости реакции – м3/(моль*с), когда концентрации веществ и количество актов реакции измеряются не в штуках, а в молях на м3.
Если реакция имеет вид A+B→C+D, то

Здесь k – константа скорости реакции. Для реакции второго порядка размерность константы должна быть [м3/(моль*с)]. Второй порядок означает, что в реакции принимают участие два реагента, а на микро-уровне акт реакции происходит с некоторой вероятностью, когда происходит столкновение молекул двух реагентов.
Порядок реакции может быть произвольным. Для порядка N:
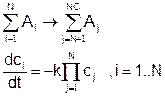
а размерность константы скорости реакции должна быть: [м3(N-1)/( мольN-1*c], тогда в уравнении закона действующих масс размерности правой и левой частей совпадают. Здесь NC – общее количество компонент смеси, включая как реагенты, так и продукты реакции.
Наибольшую скорость обычно имеют реакции второго порядка, поскольку столкновение двух частиц значительно более вероятно, чем трех и более. В принципе могут иметь место реакции первого порядка, которые, в отличие от других порядков, вообще не связаны со столкновениями.
Если концентрации частиц измерять не в молях на м3, а в частицах на м3, то размерность константы скорости второго порядка – [м3/с]. Для произвольного порядка: [м3(N-1)/c].
Константа скорости реакции k связана с сечением реакции s следующим образом:
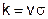
где v – средняя тепловая скорость движения молекул. То есть если размерность концентраций – [1/м3], а константы скорости реакции второго порядка - [м3/с], то размерность сечения реакции – [м2], что вполне естественно.
Если размерность концентраций – [моль/м3], а константы скорости реакции второго порядка - [м3/(моль*с)], то размерность сечения реакции – [м2/моль]. Это уже не так естественно, но так уж есть.
Еще один вариант: когда основная система единиц – СГС, то концентрации измеряются в молекулах на кубический сантиметр ([1/см3]), константы скорости реакций второго порядка – в [см3/с], а сечения реакций – в [см2].
Формулы для пересчета значений константы скорости приведены в таблице 1. В заголовках строк и столбцов – размерности констант скорости реакций второго порядка, в ячейках – множители, на которые нужно умножить константу скорости для пересчета ее из размерности строк в размерность столбцов.
Таблица 1. Пересчет констант скорости реакций второго порядка.
| м3/(с× моль) | см3/(с× моль) | м3/с | см3/с | |
| м3/(с× моль) | 1 | 106 | 1/NA | 106/NA |
| см3/(с× моль) | 10-6 | 1 | 10-6/NA | 1/NA |
| м3/с | NA | 106NA | 1 | 106 |
| см3/с | NA/106 | NA | 106 | 1 |
Таблица 2. Соответствие размерностей концентраций и констант скорости реакций второго порядка.
| Концентрации | Константы |
| моль/м3 | м3/(с× моль) |
| моль/см3 | см3/(с× моль) |
| 1/м3 | м3/с |
| 1/см3 | см3/с |
– Конец работы –
Эта тема принадлежит разделу:
Термодинамика. Конспект лекций
Термодинамика активных сред химических лазеров. Конспект лекций. Составитель: Д.т.н., профессор А.В. Савин...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Кинетика активной среды кислородно-йодного лазера
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов